
Desafios da Verificação Continuada de Processo
Atualmente vivemos em um momento de grande renovação regulatória frente a harmonização da ANVISA – Agência Nacional de Vigilância Sanitária com o PIC/s –Pharmaceutical Inspection Co-operation Scheme. Com isso, muitos conceitos já implementados em outros países, passam a ser utilizados e requeridos dentro da nova legislação nacional.
Dentre as grandes mudanças relacionadas a publicação da RDC 301/2019 de boas práticas de fabricação de medicamentos, bem como com a IN 47/2019 instrução normativa complementar às boas práticas de qualificação e validação, trouxeram uma nova abordagem conceitual que exigem um aprofundamento e maior conhecimento dos processos produtivos e consequentemente das características dos produtos fabricados pelo fornecedor.
Sendo assim, destaca-se dentro da IN 47/2019, o Art. 45 que traz claramente a seguinte definição:
A abordagem de validação de processos deve:
I – interligar o desenvolvimento de produtos e de processos;
II – garantir a validação de processo de fabricação comercial;
III – manter o processo em um estado de controle durante a produção comercial de rotina.
Frente ao exposto, pode-se interpretar o referido artigo como sendo a nova estratégia a ser contemplada para o ciclo de vida do produto, a qual pode ser entendida da seguinte forma:
Figura 1 – ABORDAGEM DE VALIDAÇÃO DE PROCESSOS

Mas o que seria Ciclo de Vida do Produto?
Conforme o Art. 3º V da Instrução Normativa IN 47/2019,temos a seguinte abordagem para o ciclo de vida – Todas as fases da vida útil de um produto, equipamento ou instalações, desde o desenvolvimento inicial ou até a descontinuação do uso. Sendo está também a abordagem realizada pelo ICH Q8 – International Conference Harmonization.
Por sua vez, o Guidance for Industry – Process Validation: General Principles and Practices do FDA, diz que o conceito de ciclo de vida vincula o desenvolvimento de produtos e processos, a qualificação comercial do processo e a manutenção do processo em um estado de controle durante a rotina de produção comercial até sua descontinuação.
Dentre as normativas que trazem a abordagem do ciclo de vida do produto, o PDA Task Force on Technical Report No. 60: Process Validation: A Lifecycle Approach, traz uma abordagem mais ampla sobre o assunto, ajudando a obter um melhor entendimento do mesmo.
Desse modo, o Ciclo de Vida do Produto é divido em três principais fases, sendo estas:
Fase 1 – Desenvolvimento do processo
- Definição do perfil do produto alvo e perfil de qualidade do produto alvo – QTTP;
- Identificação dos ACQ’s (atributos críticos de qualidade);
- Definição do processo.
– Caracterização do Processo
- Avaliação de risco – Categorização de Parâmetros;
- Experimentos de caracterização de processo (DOE, multivariada, univariada)
- Categorização final de parâmetros embasada na criticidade e estabelecimento da estratégia de controle.
Fase 2 – Qualificação do Processo
- Implementação da estratégia de controle de processo;
- Qualificação de instalação, utilidade e equipamento;
- Qualificação de desempenho do processo;
Fase 3 – Verificação Continuada do Processo
- Manutenção do status validado
Diante da nova abordagem do ciclo de vida do produto, o objetivo é manter o processo em estado de controle durante toda a vida produtiva, até sua descontinuação.
Figura 2 – FASES DO CICLO DE VIDA DO PRODUTO

E com a inserção desse novo conceito, veio um dos grandes desafios para as indústrias farmacêuticas, que é a Fase III de Validação de Processos – Verificação Continuada do Processo.
Em que consiste essa nova fase da validação?
A Verificação Continuada do Processo – Fase III, consiste em avaliar a capacidade do processo em se manter dentro do seu estado de controle durante a produção comercial, mantendo desse modo, o status de validado do produto.
Mas por onde devo começar?
Primeiramente é necessário fazer uma avaliação ampla dos requerimentos regulatórios, para que em seguida consiga avaliar os mesmos frente as condições da empresa.
Quais os principais apontamentos os requerimentos regulatórios trazem?
Conforme verificado em alguns guias e legislações como ANVISA, PDA, WHO, FDA, ISPE, ICH e EMA.
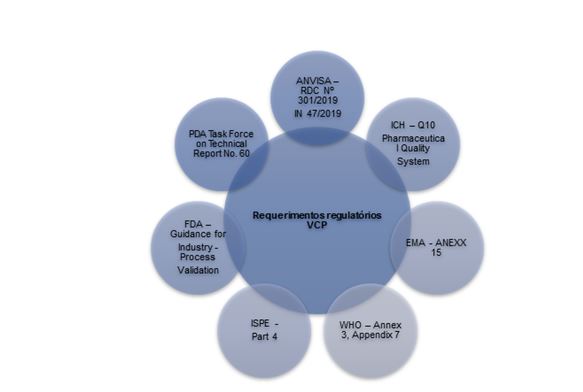
Em um contexto geral, todas essas normativas trazem como principais premissas a implementação de uma avaliação da capacidade do processo, avaliação de tendências, realização do monitoramento em tempo real, estado de controle do processo, melhores ações preventivas e corretivas, melhoria contínua dos processos.
Para isso, faz-se necessário desenvolver e implementar uma estratégia que permita extrair essas informações e aplicá-las ao seu processo, sendo essa a tarefa mais difícil de toda essa avaliação, pois exige um conhecimento amplo dos processos e conhecimentos das limitações da empresa.
Neste momento será necessário definir o planejamento dessa nova atividade dentro do sistema da qualidade da empresa, e para isso um plano mestre precisará ser elaborado, de modo a contemplar:
- Áreas envolvidas e suas responsabilidades,
- As estratégias de amostragem e testes,
- Métodos de análise dos dados (ferramentas estatísticas),
- Critérios de aceitação,
- Avaliação de tendências,
- Tratativa de desvios.
Vale destacar ainda que para um Plano de Verificação Continuada será necessário definir qual a estratégia será estabelecida pela empresa tanto para os produtos legados, que são os produtos pertencentes a empresa que já se encontram em comercialização, quanto para os novos produtos que passarão a fazer parte do portifólio da empresa.
Por sua vez no Capítulo III, da IN 47/2019, temos o Art.131 que diz:
A aplicação da Verificação Continuada de Processos a produtos legados depende das conclusões do Sistema de Gestão da Qualidade Farmacêutica quanto ao estado de controle destes produtos.
Parágrafo único. Pode vir a ser necessária a verificação continuada dos processos produtivos de produtos legados que não estejam dentro do estado de controle e, por consequência, tiveram o monitoramento continuado de suas fontes de variação determinada, por força de monitoramento extensivo ou redesenho de seus processos.
Com isso, a empresa também precisará ter uma estratégia concisa sobre quais mudanças e/ou tendências poderão impactar no status de validado do produto, de modo que este precise retornar para a Fase 1 (Desenvolvimento) e/ou Fase 2 (Qualificação do Processo), seguindo posteriormente para a Fase 3 de Verificação Continuada do Processo.
No Technical Report Nº. 60: Process Validation: A Lifecycle Approach, é apresentada uma proposta para avaliação dos produtos legados, onde é apresentado o fluxograma abaixo:
Figura 3 – Determinação do Plano CPV para produtos legados
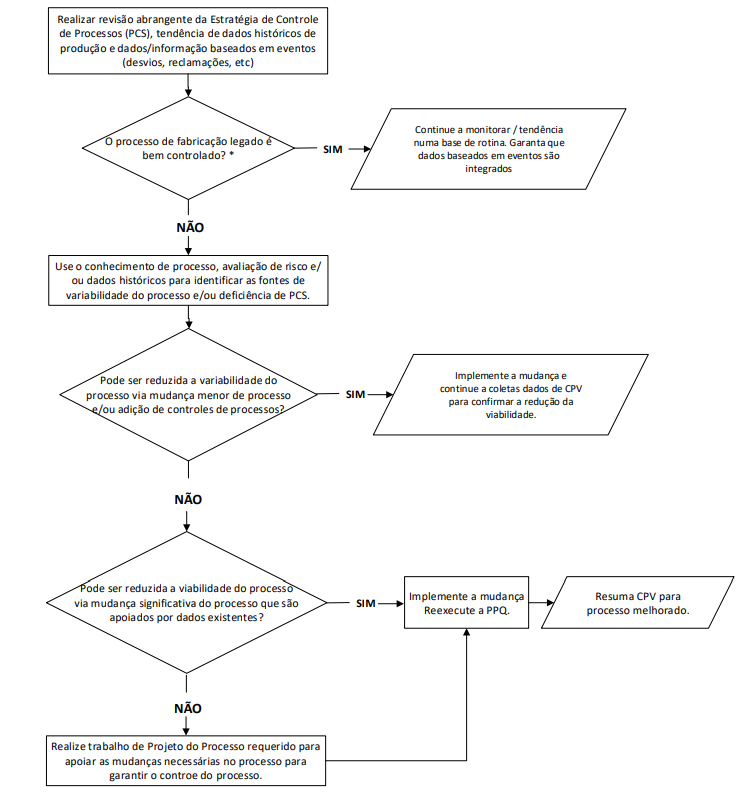
*Uma Estratégia de Controle de Processo (demonstrando compreensão do impacto dos parâmetros de processo no CQAs) está definida e feita a estatística dos dados mostram que a variabilidade é controlada?
Para a definição da estratégia de avaliação dos produtos legados, é muito importante ser realizada uma avaliação de risco, para entender quais serão os produtos que iniciarão o monitoramento on going.
Produtos que possuem alta demanda produtiva, produtos que possuem maior número de desvios e produtos que apresentam alta variabilidade são opções válidas como primeiras escolhas. Mediante ao cenário mapeado, deve-se definir a prioridade para o monitoramento.
Para as empresas que possuem um portifólio amplo, com uma grande gama de produtos, porque não se basear no cronograma de RPP?
Essa pode ser uma ótima forma de iniciar os monitoramentos on going de seus produtos legados. Como existe uma dificuldade de definirmos um cronograma e como a atividade de RPP já possuí um cronograma anualmente definido de avaliação dos produtos esse pode ser um ótimo ponto de partida para iniciados os estudos.
O mais importante, nesse momento, é que cada empresa entenda o seu cenário, e diante deste cenário extraia e defina qual seria a melhor estratégia a ser pleiteada, sempre embasado em uma avaliação de risco e no conhecimento científico.
Para Novos Produtos, sendo esses em fase de desenvolvimento a partir da vigência da RDC 301/2019, precisam ser lançados já em conformidade com o conceito de Quality by Desgin, onde o fabricante passa a ser cobrado de um conhecimento mais amplo de seus processos / produtos desde a fase inicial de desenvolvimento até a descontinuação desse.
No Technical Report Nº. 60: Process Validation: A Lifecycle Approach, é apresentado uma proposta que aborda todas as fases do ciclo de vida, iniciando sempre na fase de desenvolvimento do produto, conforme pode ser observado na figura abaixo.
Figura 4 – Determinação do Plano CPV para novos produtos

A verificação continuada do processo – VCP, é uma novidade para grande parte das indústrias nacionais. Porém, avaliando as datas de vigência e/ou publicação das normas que abordam esse tema, observamos que essas não são propostas novas e/ou recém desenvolvidas para a área industrial, estando essas em desenvolvimento e amadurecimento, buscando sempre aplicar uma avaliação dos processos por parte do fabricante por toda a vida do seu produto, pois essa abordagem visa a melhoria e a qualidade continua dos processos e dos produto fornecidos.
Então agora vem a próxima parte, planejar e implementação a sua verificação continuada do processo – VCP e neste momento precisamos sempre ter em mente as principais premissas relacionadas a essa atividade, sendo essas:
Figura 5 – Principais premissas para a verificação continuada do processo
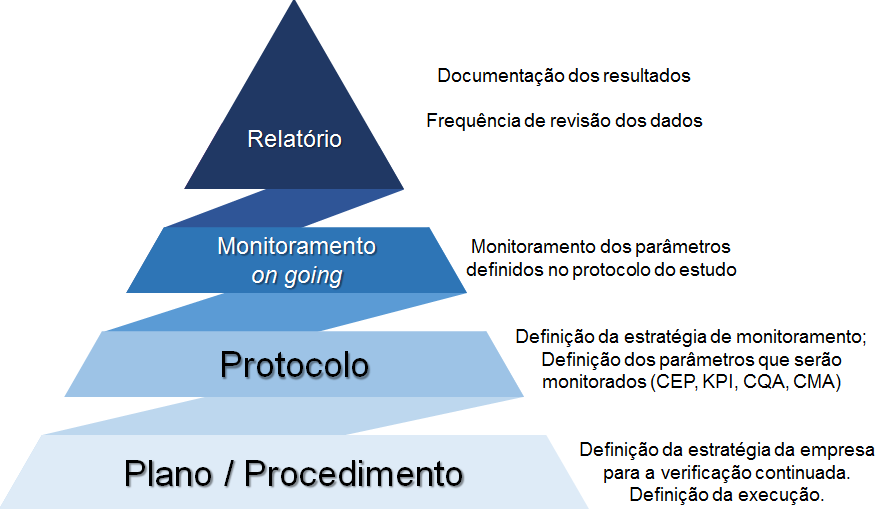
Após definida a estratégia de monitoramento, estabelecido os parâmetros que serão monitorados e as avaliações estatísticas que serão aplicadas ao estudo, entramos assim no momento relacionado ao processo de coleta os dados.
E quantos dados devem ser coletados?
A coleta de dados deverá sempre ser em quantidade suficiente para realizar as avaliações estatísticas definidas no seu protocolo, sendo orientado pelos guias a necessidade de um número mínimo de 20 dados e no máximo de 30 dados.
Esse número de dados sugeridos vem alinhado a estratégia de implementação de ferramentas estatísticas, atendendo consequentemente ao Art. 78 da IN 47/2019, onde:
Os fabricantes devem monitorar a qualidade dos produtos para assegurar que o estado de controle é mantido durante todo o ciclo de vida.
Parágrafo único. As tendências relevantes do processo devem ser avaliadas
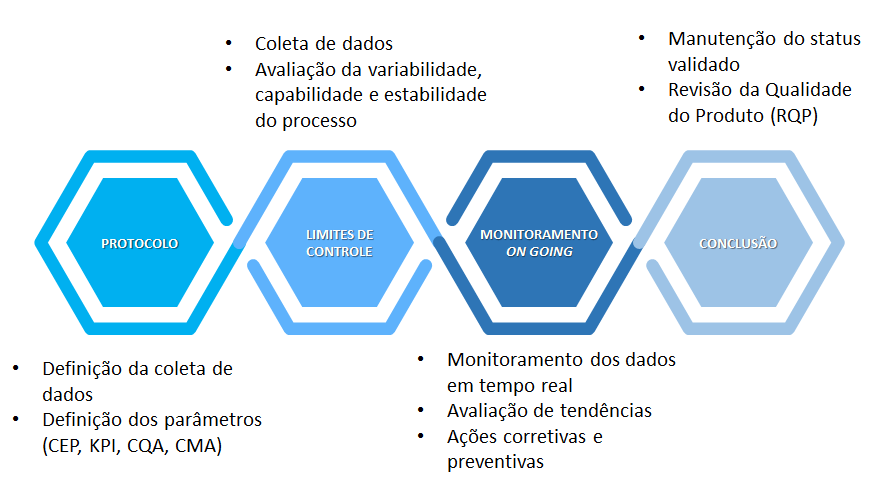
Frente a todo o contexto apresentado nos guias disponíveis, podemos resumir que as estratégias para superarmos os desafios relacionados a implantação de uma Verificação Continuada de Processos devem sempre estar alinhadas aos cenários da empresa, bem como aos requerimentos regulatórios. A figura abaixo traz o resumo de todo o ciclo abordado:
Figura 6 – Pontos importantes para a implementação da Verificação Continuada do Processo.
REFERÊNCIAS
- ANVISA – RDC Nº 301/19 – Boas Práticas de Fabricação de Medicamentos
- ANVISA – Instrução Normativa – IN Nº 47– Boas Práticas de Fabricação de complementar às boas práticas de qualificação e validação
- WHO – World Health Organization – Annex 3, Guidelines on good manufacturing practices: validation, Appendix 7: non-sterile process validation, item 6: Continued Process Verification
- ICH – International Conference Harmonization – Q10 Pharmaceutical Quality System – Item 3.2.1: Process Performance and Product Quality Monitoring System
- FDA – Guidance for Industry – Process Validation: General Principles and Practices Item IV – B: Continued Process Verification
- EMA – European Medicines Agency – Guidelines for Good Manufacturing Practice for Medicinal Products for Human and Veterinary Use – Annex 15: Qualification and Validation: On going Process Verification during Lifecycle
- PDA – Parenteral Drug Association – Task Force on Technical Report No. 60: Process Validation: A Lifecycle Approach
Escrito por:
Gesane dos Santos Afonso Abreu:
Farmacêutica generalista, formada pela Fundação Hermínio Ometto – FHO. Atuante na área industrial farmacêutica desde 2015 na área de Garantia da Qualidade com foco voltado para as atividades de Qualificação e Validação. Atuando na área de validação de processo dentro das indústrias lifescience sendo participante ativa dos grupos de mentoria Premium, Platinum e do Instituto de Qualidade e Validação – IQQV de Daniela Silva – MD Consultoria.


